В начале 1990-х годов группа японских ученых во главе с Тасуку Хондзе обнаружила белок, названный PD-1, или белок запрограммированной смерти клеток¹. Спустя десятилетия, в 2018 году, доктор Хондзе и его американский коллега Джеймс П. Эллисон, параллельно открывший близкий по функциям белок, получили за это Нобелевскую премию за достижения в области физиологии и медицине.
Опухолевые клетки появляются в нашем организме постоянно, но иммунная система блокирует их и не позволяет раку развиваться. Это происходит так.
Почти все клетки в организме в процессе обмена веществ производят белки и сообщают об этом иммунной системе, располагая на своей поверхности фрагменты этих белков. Такие «отпечатки» называются белками главного комплекса гистосовместимости. Раковые же клетки синтезируют ненормальные белки. Иммунитет их распознает, и опухоль уничтожается еще в зачатке. Более подробно читайте в этом материале.
Однако, несмотря на такой строгий контроль, в организме человека все же развиваются опухоли. Значит, у злокачественных клеток есть инструменты, позволяющие скрыться от иммунитета. Именно этой проблемой и занималась команда доктора Хондзе.
На поверхности активированных Т-киллеров — основных охранников иммунной системы, уничтожающих чужеродные клетки, — ученые обнаружили рецептор PD-11. Если воздействовать на него белком (лигандом) PD-L1, организм запускает механизмы естественной смерти клеток для предотвращения чрезмерной активности иммунитета. Но злокачественные клетки научились использовать эти механизмы в своих целях. Исследователи обнаружили на поверхности клеток многих опухолей лиганд PD-L1, белковую молекулу, которая связывается с рецептором PD-1 и подавляет активность иммунитета. Таким образом опухоль «прячется» от иммунной системы.
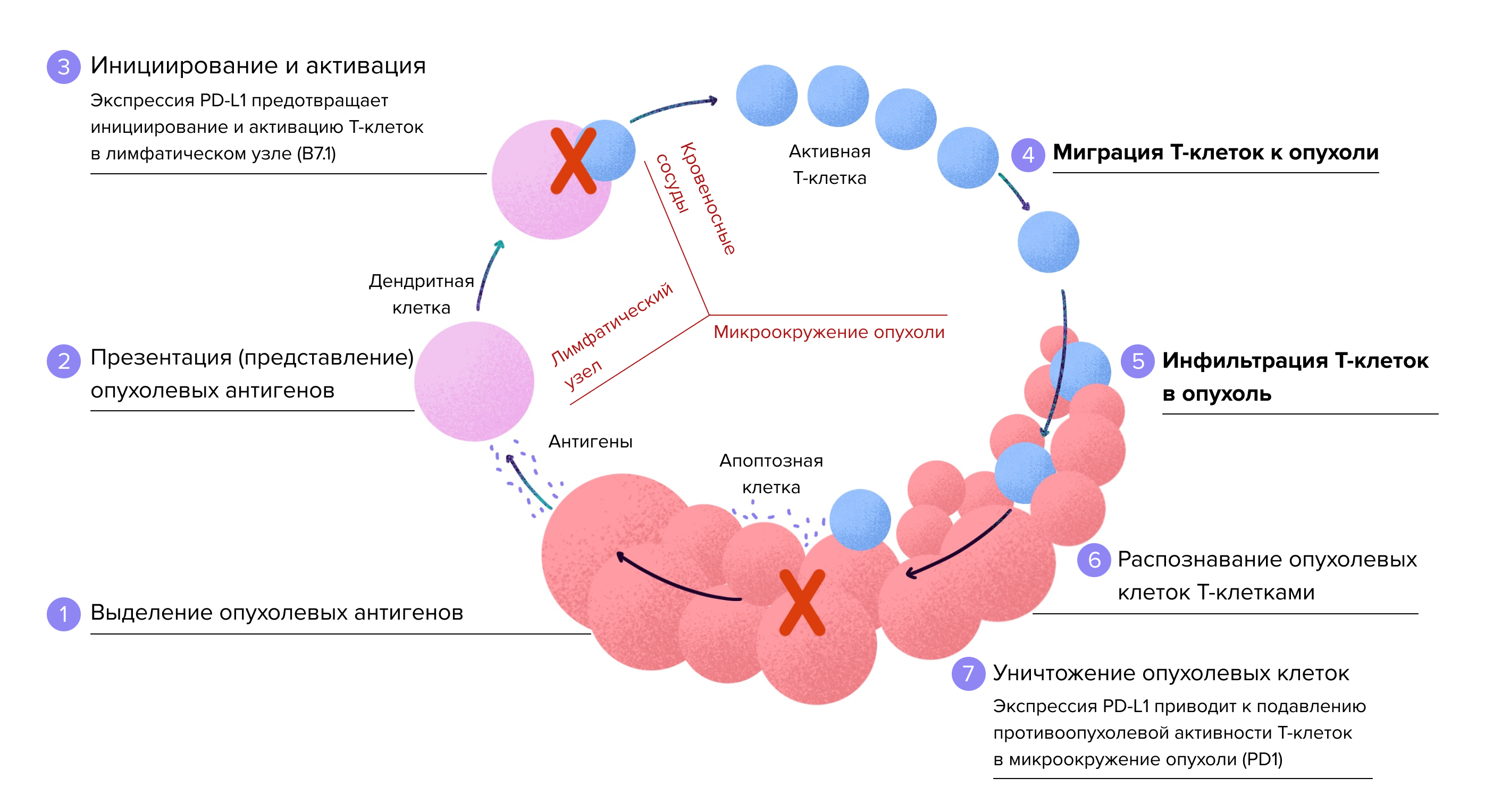
После нескольких лет исследований ученые пришли к выводу, что блокирование рецептора PD-1 или белка PD-L1 приведет к активации иммунной системы человека, которая начнет «видеть» опухолевые клетки. Эти данные помогли разработать новые лекарственные препараты и вывести иммунотерапию на новый уровень. Сегодня врачи используют несколько видов иммунотерапии в лечении многих злокачественных новообразований. Однако наилучшие результаты получены у пациентов с распространенной меланомой и раком легкого при использовании блокаторов PD-L1/PD-1. Изучается возможность использования препаратов этой группы у больных после операции по поводу локализованных форм рака.
Иммунотерапия немелкоклеточного рака легкого
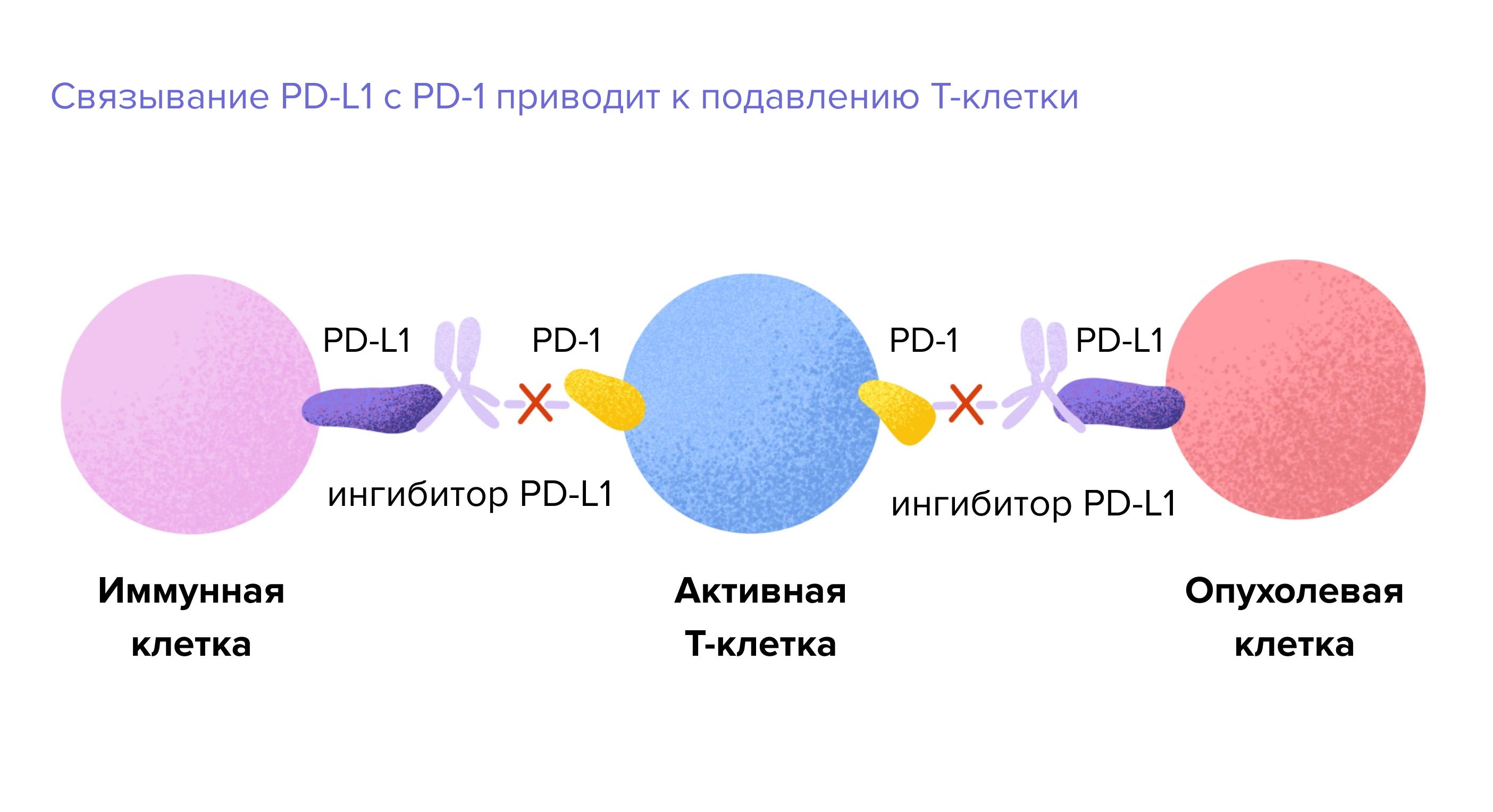
Как работает такая терапия? Ученые создали два класса препаратов, которые используются при иммунотерапии рака легкого: одни блокируют сам рецептор PD-1 на иммунных клетках, другие — его лиганд PD-L1 на раковых клетках. Их задача — разорвать связь между рецептором PD-1 и его лигандом PD-L1 на опухолевой клетке, благодаря чему опухолевая клетка перестанет тормозить клетки иммунного надзора и станет беззащитной для них. Эти лекарства представлены в виде моноклональных антител ( защитных белков, синтезированных в лаборатории).
Ингибиторы PD-1/PD-L1 можно применять несколькими способами:
- в качестве препаратов первой линии терапии метастатического немелкоклеточного рака легкого;
- в комбинации с химиотерапией, ангиогенной и лучевой терапией;
- после неудачной первой линии химиотерапии в качестве препаратов второй линии².
Несколько исследований показали, что препараты этой группы в комбинации с препаратами иммунотерапии другого класса достоверно снижают прогрессирование опухоли, увеличивают продолжительность жизни по сравнению с плацебо и эффективнее (более продолжительная средняя выживаемость), чем стандартная схема химиотерапии. При их приеме наблюдается несколько меньшее количество осложнений, чем при стандартной схеме химиотерапии³'⁴'⁵.
Сейчас иммунотерапия считается стандартом первой линии терапии рака. При этом потенциальным прогностическим признаком успешности иммунотерапии считается экспрессия (представленность) лиганда PD-L1 на поверхности раковых клеток. Этот показатель рассчитывается во время иммуногистохимического исследования: клетки опухоли обрабатывают специальным красителем, а затем подсчитывают процент окрашенных клеток к их общему числу. В зависимости от уровня экспрессии PD-L1 на поверхности раковых клеток врач может назначить только моноиммунотерапию (при высоком уровне экспрессии), либо иммунотерапию в сочетании с химиопрепаратами (при низкой или отрицательной экспрессии). При этом врач обязательно оценивает общее состояние пациента и его возможную реакцию на комбинированную терапию.
Иммунотерапия наряду с таргетной стала прорывом в лечении метастатического рака легких. На данный момент это современный и эффективный метод 1-й линии терапии пациентов с немелкоклеточным раком легкого, у которых не обнаружено EGFR\ALK и других клинически значимых драйверных мутаций. Поэтому крайне важно своевременно выполнять анализ на определение экспрессии PD-L1 с целью определить возможность назначения блокаторов контрольных точек иммунитета в монорежиме или комбинации с химиотерапией. Это позволит продлить жизнь и сохранить ее качество.
Литература:
- Ishida Y., Agata Y., Shibahara K., Honjo T. Induced expression of PD-1, a novel member of the immunoglobulin gene superfamily, upon programmed cell death, EMBO J., 11(11), pp. 3887-3895, 1992. (Электронный ресурс). URL: https://pubmed.ncbi.nlm.nih.gov/1396582/ (дата обращения: 20.02.2021 года).
- Клинические рекомендации “Злокачественное новообразование бронхов и легкого”, 2020 год. (Электронный ресурс). URL: https://oncology-association.ru/wp-content/uploads/2020/12/rak-legkogo_02.pdf (дата обращения: 20.02.2021 года).
- Suresh K., Naidoo J., Lin C.T. et al. Immune Checkpoint Immunotherapy for Non-Small Cell Lung Cancer: Benefits and Pulmonary Toxicities, Chest, Volume 154, Issue 6, Pages 1416-1423, 2018. https://doi.org/10.1016/j.chest.2018.08.1048. (Электронный ресурс). URL: https://www.sciencedirect.com/science/article/abs/pii/S0012369218323365 (дата обращения: 21.02.2021 года).
- Malhotra J., Jabbour S.K., Aisner J. Current state of immunotherapy for non-small cell lung cancer, Transl Lung Cancer Res., 6(2), 196–211, 2017. doi: 10.21037/tlcr.2017.03.01. (Электронный ресурс). URL: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5420529/ (дата обращения: 21.02.2021 года).
- Doroshow D.B., Sanmamed M.F., Hastings K. et al., Immunotherapy in Non−Small Cell Lung Cancer: Facts and Hopes, Clin Cancer Res; 25(15), pp. 4592 - 4602, August 1, 2019. DOI: 10.1158/1078-0432.CCR-18-1538. (Электронный ресурс). URL: https://clincancerres.aacrjournals.org/content/clincanres/25/15/4592.full.pdf (дата обращения: 21.02.2021 года).
M-RU-00004771 октябрь 2021

